


骨肉瘤是恶性程度很高的原发性骨肿瘤,发病人群集中在儿童和青少年,尚无特异治疗靶标。表观遗传修饰-转录调控过程的紊乱是骨肉瘤的重要特征之一,与肿瘤的发生发展密切相关。但目前仍无有效的表观遗传调控分子或转录因子作为靶标用于骨肉瘤的诊治,对其如何影响骨肉瘤发生发展、在肿瘤中如何被调控等过程也缺乏深入和系统的研究。

2023年11月22日,华南恶性肿瘤防治全国重点实验室康铁邦研究团队在Science Advances发表题为《增强多梳蛋白L3MBTL2诱导的凝聚体可抑制骨肉瘤的生长》的论文(点击阅读原文),揭示多梳蛋白L3MBTL2通过液-液相分离凝聚非经典多梳蛋白复合体PRC1.6来实现对靶基因的调控,发挥其转录沉默以及抑癌的功能。研究还发现砒霜活性成分(三氧化二砷)可促进L3MBTL2蛋白累积形成更多核内凝聚体,增强其转录沉默活性,最终抑制肿瘤生长。
该研究通过表观遗传分子与转录因子的CRISPR-Cas9文库筛选、细胞功能实验、小鼠模型以及临床样本验证,在骨肉瘤中鉴定了一个新的抑癌基因L3MBTL2,其可抑制骨肉瘤细胞的增殖与肿瘤生长,L3MBTL2蛋白低表达与骨肉瘤患者不良预后显著正相关。研究人员进一步发现L3MBTL2的结合功能域Pho-binding pocket和C端polybasic region (PBR) 可介导其通过液-液相分离,招募PRC1.6复合体的其他亚基,在核内形成生物分子凝聚体,增强其转录抑制活性,沉默TNF/NF-kB信号通路相关基因(IFIT2等)表达,从而发挥其抑癌功能。
接下来,研究人员试图探明L3MBTL2在骨肉瘤细胞中如何被调控。通过BioID邻近标记以及串联亲和纯化(TAP)联合质谱分析,研究人员发现E2/E3杂合酶UBE2O特异性结合L3MBTL2蛋白C端的PBR,促进L3MBTL2蛋白通过多位点单泛素化-蛋白酶体途径而降解。砒霜活性成分(三氧化二砷)可通过抑制UBE2O促进L3MBTL2蛋白累积,形成更多生物分子凝聚体,进而抑制骨肉瘤的生长。
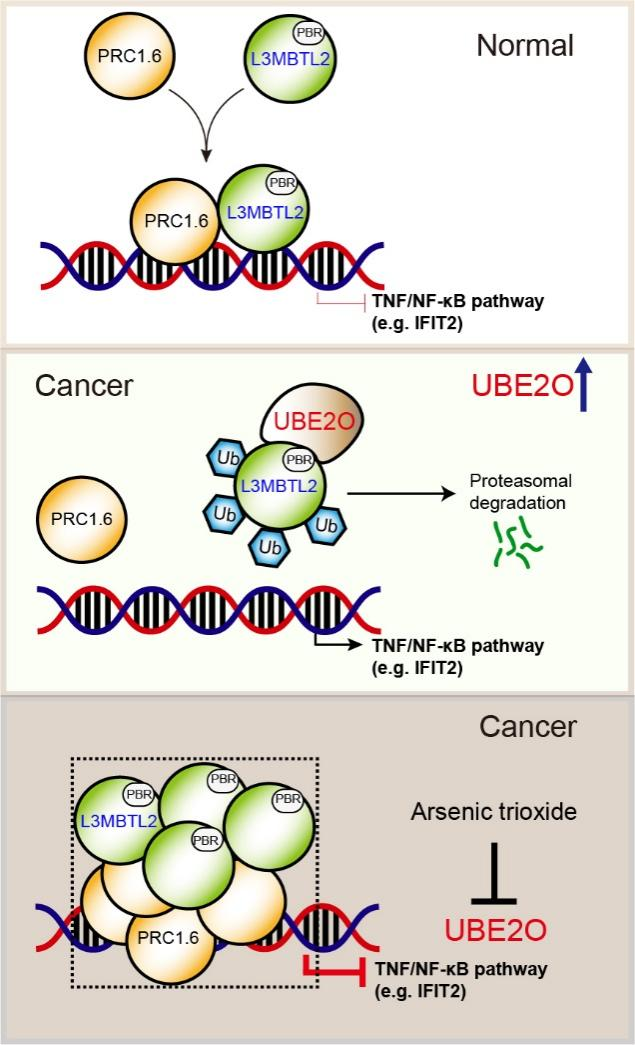
L3MBTL2-PRC1.6凝聚体在骨肉瘤中的作用及调控机制模型图
该研究揭示了L3MBTL2是抑癌基因,其蛋白是PRC1.6复合物的重要成分,调控NF-kB通路。在肿瘤(比如,骨肉瘤)中,UBE2O表达增加,从而降解L3MBTL2,活化NF-kB通路,有利于肿瘤存活。三氧化二砷可抑制UBE2O活性,导致L3MBTL2蛋白累积,形成生物分子凝聚体,增强转录沉默活性并抑制肿瘤生长。该研究结果表明,增强具有抑癌活性的生物大分子凝聚体形成,可作为治疗肿瘤的新策略。“复方黄黛片(三氧化二砷)联合顺铂治疗标准治疗后失败的骨肉瘤患者的临床研究”,目前正在中山大学附属第一医院骨肿瘤科进行。
中山大学肿瘤防治中心/华南恶性肿瘤防治全国重点实验室康铁邦研究员、廖丹副研究员、中山大学附一院尹军强教授为共同通讯作者。中山大学附属第七医院钟理副研究员、中山大学肿瘤防治中心博士研究生汪璟璇、中山大学附属第七医院硕士研究生陈婉琪为共同第一作者。