


6月26日,国际转化医学顶级期刊《科学转化医学》(Science Translational Medicine)在线发表了华南恶性肿瘤防治全国重点实验室邓蓉、朱孝峰团队的最新成果:TRPML1介导铁死亡抵抗是AKT高度激活肿瘤的潜在治疗靶标(点击查看)。该研究首次证实了TRPML1-ARL8B介导的溶酶体胞吐导致铁死亡耐受及其分子机制,揭示了肿瘤潜在治疗策略。
细胞死亡抵抗是肿瘤十四大特征之一。铁死亡(Ferroptosis)是铁依赖的脂质过氧化驱动的程序性细胞死亡方式。铁死亡在肿瘤的发生发展中扮演着重要角色。近些年的研究表明,诱导铁死亡是极具潜力的肿瘤治疗方式。
邓蓉、朱孝峰团队长期以来致力于铁死亡调控机制及其在肿瘤发生发展和治疗中的作用的研究。他们发表在Nature Cell Biology的研究成果,发现了铁死亡的“导火索”:PKCβII通过感知脂质过氧化而激活,从而启动快速正反馈机制诱导铁死亡的发生。AKT的高度激活驱动肿瘤发生发展,以及对大多数现有标准疗法耐受,包括化疗、靶向治疗、放疗和免疫治疗,迫切需要探索新靶点及联用策略来应对此类恶性肿瘤。
针对以上临床难题,研究团队以AKT高度激活的肿瘤为模型,利用CRISPR-Cas9全基因组转录激活文库和激酶抑制剂库筛选等技术,发现溶酶体胞吐抑制肿瘤细胞铁死亡。分子机制的研究发现,AKT直接磷酸化TRPML1的Ser343位点后,能抑制TRPML1的K552泛素化和蛋白酶体降解,从而稳定TRPML1蛋白水平,增强TRPML1与ARL8B结合以触发溶酶体胞吐作用。溶酶体胞吐通过降低胞内Fe2+继而减少脂质过氧化产生,同时增强质膜修复,最终介导肿瘤细胞铁死亡耐受。首次证实了TRPML1-ARL8B介导的溶酶体胞吐导致铁死亡耐受及其分子机制,这是肿瘤细胞铁死亡抵抗新模式。
随后,研究人员深入探讨了溶酶体胞吐介导的铁死亡耐受在肿瘤发生和肿瘤治疗耐受中的作用。利用异种移植瘤、水动力转基因、小鼠放疗及免疫治疗等模型发现TRPML1-ARL8B介导的铁死亡抵抗是AKT驱动的肿瘤发生及肿瘤对放疗和免疫治疗耐受的重要因素。
最后,研究人员深入分析了TRPML1-ARL8B复合物形成的结构基础,进而合成了竞争性多肽。该多肽通过特异性结合TRPML1,破坏TRPML1与ARL8B的相互作用,从而阻断溶酶体胞吐促进铁死亡,抑制AKT驱动的肿瘤发生,增强AKT高度活化肿瘤对铁死亡诱导剂、放疗、免疫治疗等的敏感性,具有良好的应用前景。
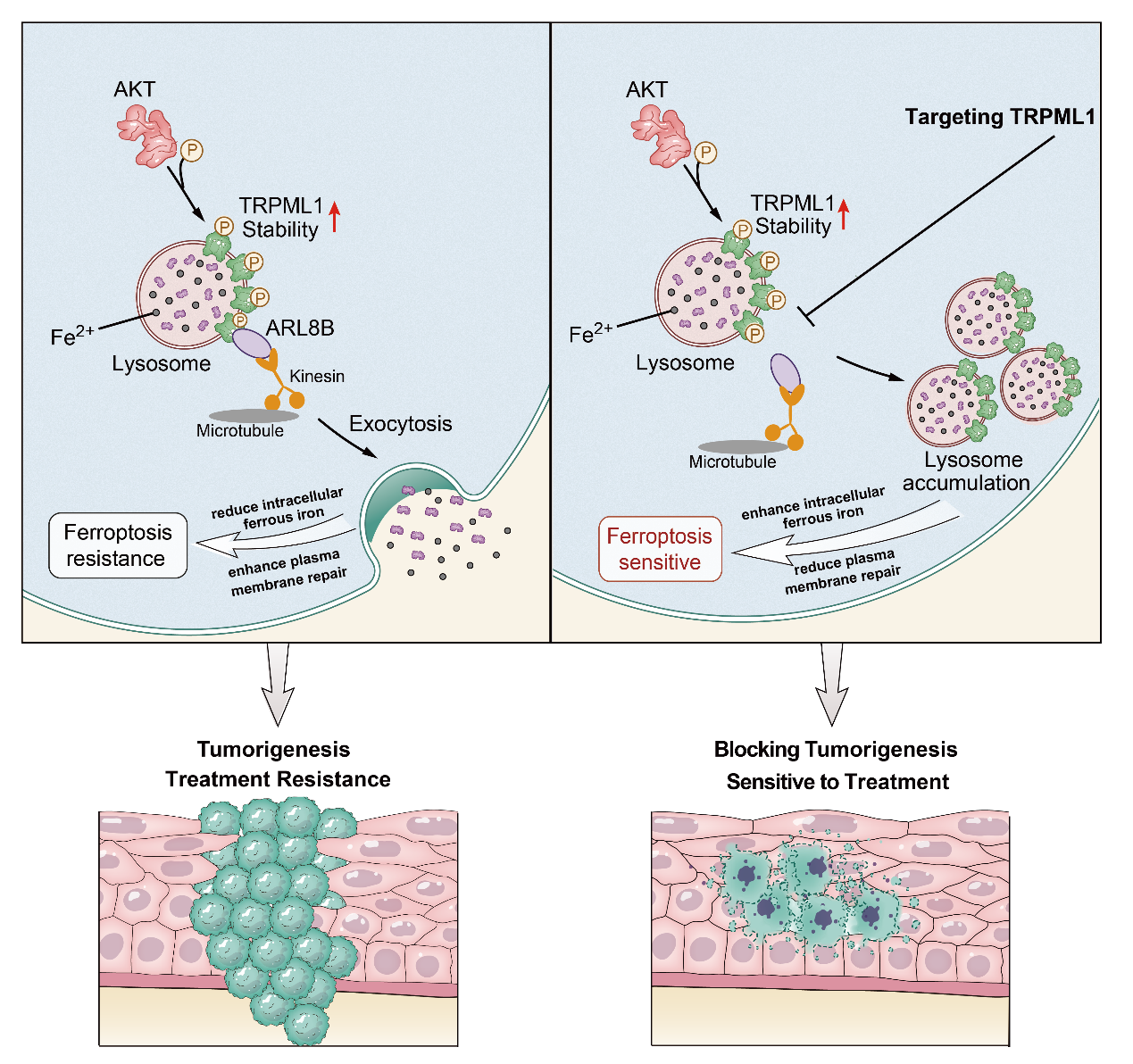
促进铁死亡抵抗的溶酶体胞吐是AKT高度激活肿瘤的治疗新靶标
本研究发现了溶酶体胞吐是新型的铁死亡抵抗系统;揭示了TRPML1-ARL8B介导的溶酶体胞吐通过抵抗铁死亡,促进AKT驱动的肿瘤发生和治疗耐受;靶向TRPML1通过抑制溶酶体胞吐促进铁死亡,是AKT驱动的肿瘤潜在治疗策略。
华南恶性肿瘤防治全国重点实验室邓蓉研究员和朱孝峰研究员是本论文通讯作者,张海亮副研究员等是本论文的第一作者。
主要研究者简介:

通讯作者 邓蓉
邓蓉,中山大学肿瘤防治中心实验研究部研究员、博士生导师、华南恶性肿瘤防治全国重点实验室学术秘书。现任中国老年保健协会肿瘤免疫治疗专委会副主任委员、中国抗癌协会抗癌药物专业委员会常务委员。长期致力于“肿瘤细胞死亡调控机制与靶向干预”的研究。以通讯/第一(含共同)发表SCI论文20余篇,包括Nature Cell Biology, Science Translational Medicine, Nature Communications, Advanced Science, Molecular Cancer, Clinical Cancer Research, Autophagy, Oncogene等国际知名肿瘤学期刊。主持包括国家自然科学基金(4项)在内的多项科研基金。

通讯作者 朱孝峰
中山大学肿瘤防治中心实验研究部主任、二级教授、博士生导师,中山大学华南恶性肿瘤防治全国重点实验室副主任,现任中国抗癌协会抗癌药物专业委员会副主任委员、中国药理学会肿瘤药理专业委员会副主任委员、中国抗癌协会肿瘤精准治疗专业委员会常务委员、中国抗癌协会肿瘤代谢专业委员会常务委员、广东省抗癌协会抗肿瘤药物专业委员会主任委员、广东省药理学会肿瘤药理专业委员会前任主任委员。主要从事肿瘤细胞死亡调控、免疫逃逸与靶向药物研究,作为通讯作者论文发表于Nature Cell Biology, Science Translational Medicine, Nature Communications,Autophagy等,申请新药发明专利12项,8项专利已获授权。主编人民卫生出版社出版的《信号转导与疾病》。