


2023年6月6日,华南恶性肿瘤防治全国重点实验室马骏研究团队、孙颖研究团队及中山大学生命科学学院邝栋明团队在Nature Medicine上发表了题为“吉西他滨联合顺铂化疗对鼻咽癌肿瘤免疫微环境的重塑作用及机制”的研究成果。研究结果将为建立鼻咽癌化疗联合免疫治疗新策略提供重要理论依据。

鼻咽癌是一种发生于鼻咽部上皮细胞的恶性肿瘤,高发于中国。2019年,马骏、孙颖教授牵头多中心单位开展了一项吉西他滨联合顺铂诱导化疗(下面简称“GP化疗”)治疗局部晚期鼻咽癌的大型前瞻性Ⅲ期临床试验,采用GP化疗可将局部晚期鼻咽癌患者的长期生存率从76.5%提高至85.3%。目前,GP化疗被美国、欧洲、中国指南等以最高等级推荐为全球标准治疗方案。已有证据表明,化疗药物不仅可以直接杀伤肿瘤细胞,还具有免疫调节作用。那么,GP化疗这一临床“高效低毒”治疗方案是否以及如何调控鼻咽癌患者的抗肿瘤免疫,目前尚不清楚。
该研究发现,GP化疗介导的肿瘤细胞DNA片段释放可通过Toll-like receptor 9(TLR9)信号诱导CD27+IgD+IgM+先天样B细胞亚群(innate-like B cell, ILB),该亚群定位于化疗诱导的类三级淋巴样结构中,通过ICOSL-ICOS信号轴促进I型辅助性T细胞(TH1)和滤泡辅助性T细胞(TFH)的扩增,进而促进细胞毒性CD8+ T细胞(Cytotoxic T Lymphocyte, CTL)的杀伤功能;与此同时,其还可激活肿瘤细胞的STING-type-I-interferon通路,进而上调肿瘤细胞主要组织相容性复合体(major histocompatibility complex, MHC)class I的表达。二者形成环路,最终,激活的免疫系统有效识别和杀伤鼻咽癌细胞。这项研究阐明了化疗免疫调节作用的新机制,提出了以B细胞为核心的抗肿瘤免疫网络新理论,研究结果将为建立鼻咽癌化疗联合免疫治疗新策略提供重要理论依据。
研究团队利用单细胞转录组测序和免疫组库测序,分析了15例鼻咽癌患者GP化疗前后的配对肿瘤组织,共计30例样本,发现GP化疗后肿瘤中CD8+ T细胞的杀伤功能显著增强。有意思的是,经典的抗原递呈细胞-树突状细胞(Dendritic cells, DCs)的比例并未显著增加,且处于功能抑制状态;巨噬细胞的比例同样不增反降。同时,研究人员观察到,化疗后肿瘤中B淋巴细胞的浸润水平显著增加。B淋巴细胞和T淋巴细胞共同组成了机体的适应性免疫系统。一方面,激活后分化成熟的B细胞可通过分泌特异性抗体响应感染和肿瘤等疾病,另一方面,B细胞也可作为抗原递呈细胞启动T细胞的特异性免疫反应。那么,B细胞是否是调控化疗后的抗肿瘤免疫网络的关键细胞群呢?
进一步研究发现,化疗后CD27+IgD+IgM+ B细胞亚群(ILB)的比例显著富集;并且,组织中ILB细胞的比例与患者的化疗响应性和远期肿瘤控制率密切正相关。接下来,研究者从鼻咽癌患者肿瘤样本中分离出ILB细胞,通过与自体肿瘤来源的T淋巴细胞进行体外共培养等实验,进一步证实GP化疗通过TLR9信号诱导ILB,ILB通过ICOSL-ICOS信号轴激活PI3K/AKT/mTOR通路促进TH1和TFH的扩增,从而增强CTL细胞的杀伤功能。此外,空间上,ILB化疗后聚集形成niche,与T细胞密切接触,并且ILB niche周围的Ki67+ T, TH1, TFH和CTL的浸润水平显著高于其他区域。有意思的是,ILB与这些效应T细胞聚集形成的结构同时表达MECA-79, CD21,CD20,CD3等经典的三级淋巴结构的标记,但缺乏生发中心。
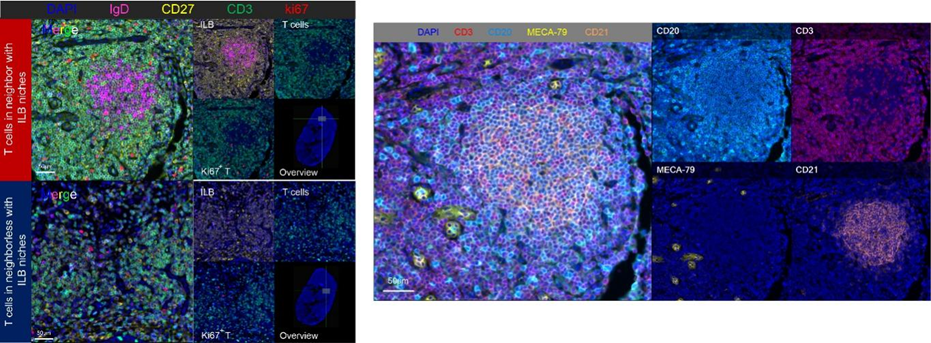
鼻咽癌患者肿瘤组织切片多色免疫荧光染色显示ILB与Ki67+ proliferating T细胞聚集,并定位于化疗诱导的“类”三级淋巴样结构中
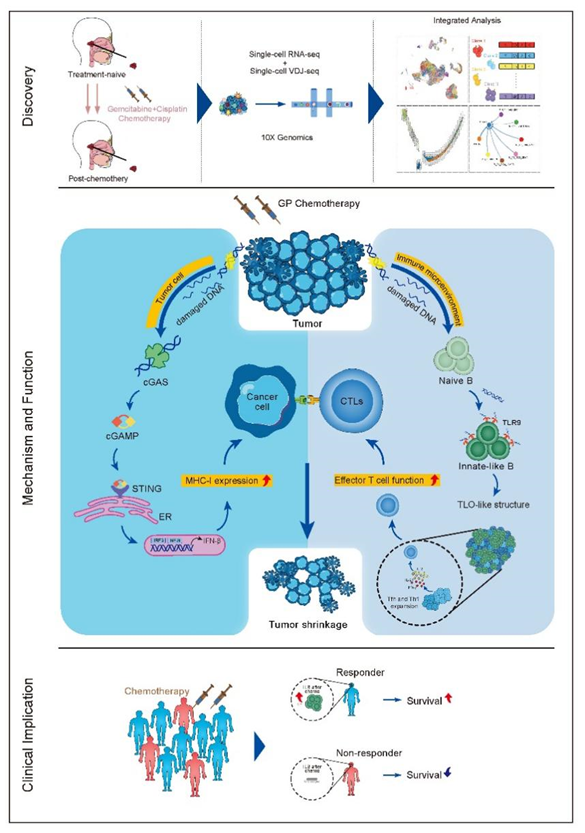
研究机制示意图
华南恶性肿瘤防治全国重点实验室马骏教授、孙颖教授、中山大学生命科学学院邝栋明教授、华南恶性肿瘤防治全国重点实验室柳娜研究员以及深圳华大基因研究所李贵波副研究员为该研究论文的共同通讯作者。吕佳蔚博士、魏瑗副教授、殷建华副研究员、陈雨沛副主任医师、周冠群副主任医师、魏晨博士、梁晓雨博士以及张媛主治医师为该研究论文的共同第一作者。
作者介绍

马骏
通讯作者
中山大学肿瘤防治中心常务副主任、副院长,教授,华南恶性肿瘤防治全国重点实验室PI,首任中国临床肿瘤学会鼻咽癌专业委员会主任委员,中国抗癌协会鼻咽癌专业委员会主任委员。以通讯作者发表高水平论文多篇,包括N Eng J Med、Lancet*2、JAMA、BMJ*2、Nat Med、Cell Res、Lancet Oncol*5、JAMA Oncol*2、J Clin Oncol等。获国家自然科学基金重点项目2项,带领团队入选“教育部创新团队、科技部重点领域创新团队”,以第一完成人获国家科技进步二等奖2项(2009、2015)、中华医学科技一等奖3项(2007、2014、2022),获何梁何利科学与技术进步奖(2022)、吴阶平医药创新奖(2020)、首届全国创新争先奖状(2017)、广东省突出贡献奖(2018)等。

孙颖
共同通讯作者
中山大学肿瘤防治中心副院长、教授,华南恶性肿瘤防治全国重点实验室PI。长期从事鼻咽癌的放射治疗及综合治疗。以通讯作者(含共同)发表高水平论文多篇,包括N Eng J Med、Lancet*2、JAMA、Nat Med、Lancet Oncol、J Clin Oncol,Radiology、Nat Commun、J Pineal Res、Cancer Res*2、Clin Cancer Res等。获主持国家重点研发计划项目1项、重大研究计划重点支持项目1项、国自然数学天元基金数学与医疗健康交叉重点专项1项,国家科技进步二等奖2项等。

邝栋明
共同通讯作者
中山大学生命科学学院教授,全国优博。以通讯作者发表高水平论文多篇,包括Immunity、Cancer Discov、Gastroenterology、J Clin Invest、Sci Adv、Hepatology、Nat Commun等。获教育部科学研究优秀成果奖一等奖、广东省自然科学技术奖一等奖和获国家自然科学奖二等奖。