


既往研究认为,化疗除了可以通过细胞毒作用直接杀伤肿瘤外,还可以通过激活cGAS-STING-干扰素信号活化肿瘤免疫,重塑肿瘤免疫微环境,募集免疫细胞间接杀伤肿瘤。因此,如何提高化疗介导的“肿瘤-免疫”唤醒效应,是提高肿瘤化疗敏感性的重要手段。
2023年9月5日,中山大学肿瘤防治中心(华南恶性肿瘤防治全国重点实验室)刘卓炜团队在国际著名权威期刊Nature communications上发表题为:“AhR通过抑制STING依赖的I型干扰素介导膀胱癌化疗抵抗”的文章(点击文末阅读原文查看)。该研究证实了化、放疗可以增强肿瘤色氨酸代谢并活化芳香烃受体(AhR),活化态AhR通过“泛素-蛋白酶体”途径降解肿瘤细胞STING蛋白并抑制了I型干扰素的产生,削弱了化疗介导的“肿瘤-免疫”唤醒效应,最终导致化疗抵抗。

氨基酸作为细胞基础代谢的必需物质在化疗介导“肿瘤-免疫”唤醒的过程中可能发挥着重要的调控作用。因此,研究人员通过氨基酸筛选模型发现色氨酸相比于其他氨基酸,显著抑制了肿瘤化疗后的免疫活化和I型干扰素分泌。随后通过一系列实验证实,抑制肿瘤色氨酸代谢或剥夺小鼠色氨酸摄取可以显著提高抗肿瘤化疗疗效。
色氨酸发挥生物学功能往往需要在体内代谢为下游产物。通过对色氨酸的代谢酶和代谢产物进行筛选分析后发现,化疗可以上调色氨酸代谢酶IDO1和色氨酸转运子SLC7A5的表达,从而增强肿瘤对色氨酸的摄取并代谢为下游产物犬尿氨酸(Kyn),随后Kyn通过活化“AhR-CUL4B-RBX1”E3泛素复合体增强对STING蛋白的降解,从而抑制了STING依赖的I型干扰素产生。
机制上,研究人员通过免疫共沉淀实验和蛋白结构分析发现,AhR主要通过“泛素-蛋白酶体”途径降解静息态的STING蛋白,并明确了关键泛素化修饰位点(K236)和泛素链形式(K48)。最后研究者发现,在膀胱癌组织中化疗介导的色氨酸代谢活化越强,患者的化疗疗效往往越差。

部分实验结果:
(A)静息态AhR与STING的结合较弱
(B)AhR被kyn活化后与STING的结合显著增强
总体而言,研究人员揭示了肿瘤色氨酸代谢抑制化疗介导的免疫活化,从而导致膀胱癌患者化疗抵抗的具体机制,丰富了化疗介导“肿瘤-免疫”唤醒的新内涵,为增强抗肿瘤化疗疗效提供了潜在新靶点。
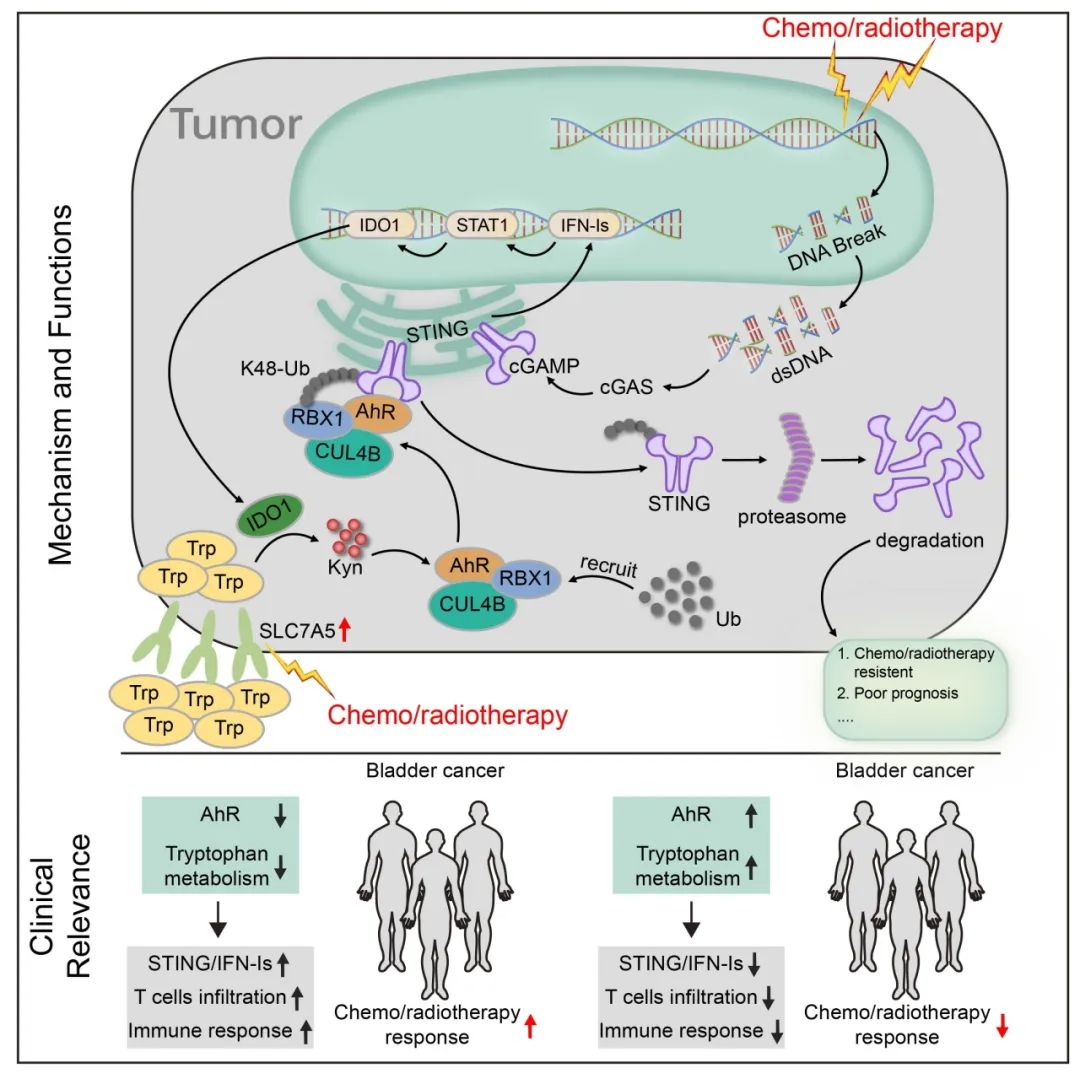
研究机制示意图
中山大学肿瘤防治中心梁晓雨医师、刘卓炜教授,中山大学生命科学学院崔隽教授为该论文的共同通讯作者。中山大学肿瘤防治中心马梓坤博士后、李志勇副主任医师、毛苡泽主治医师、叶璟威博士,中南大学湘雅医院刘泽赋博士后为该论文的共同第一作者。
通讯作者简介:

刘卓炜
中山大学肿瘤防治中心副主任、副院长,中山大学附属肿瘤医院甘肃医院执行院长,华南恶性肿瘤防治全国重点实验室PI。教授、主任医师、博士生导师。荣获中国泌尿肿瘤杰出青年奖,广东省“杰出青年医学人才”、“羊城好医生”称号,广东省医疗系统先进个人。担任中国抗癌协会肿瘤多学科诊疗专委会副主任委员、亚洲泌尿外科机器人学会(ARUS)临床研究委员会委员、中国抗癌协会科普专委会早诊早治协作组副组长、广东省医学会泌尿外科分会副主任委员、广东省医学会机器人外科学分会候任主任委员,广东省抗癌协会泌尿生殖系肿瘤专业委员会主任委员、广东省临床医学学会副会长。在Cancer Cell、Nature Communications、Cell Reports、Cancer Research、Oncogene等国际知名肿瘤学期刊上发表论文多篇。

梁晓雨
中山大学肿瘤防治中心放疗科医师。博士、博士后期间主要从事于肿瘤免疫微环境和肿瘤免疫响应信号通路方面的基础研究。以第一作者(含共同第一)或通讯作者(含共同通讯)在Cancer cell(2篇),Nature communications(2篇),Nature Medicine,British Medical Journal,Cancer Research,Biomaterials等期刊发表研究论文。主持国家自然科学基金青年基金,博士后创新人才支持计划(博新计划),博士后科学基金面上项目等。
刘卓炜教授团队长期专注于膀胱癌精准诊疗的相关研究,通过改良及程序化机器人辅助膀胱癌根治术降低了围手术期并发症,建立了高危非肌层浸润膀胱癌的综合治疗策略并提升疗效。团队围绕膀胱癌免疫应答和化疗抵抗机制发表多篇高质量论文。

课题组成员合照