


2023年6月10日,华南恶性肿瘤防治全国重点实验室徐瑞华教授、张晓实教授团队在Nature communications上在线发表题为:一项关于外周血单个核细胞来源的新抗原特异性CD8+T细胞治疗晚期实体瘤患者清淋强度的初步研究。该研究是一项探究新抗原特异性CD8+T细胞(Neo-T)治疗标准治疗难治性局部晚期或转移性实体瘤的清淋方案的单臂、开放、非随机Ⅰ期研究。研究结果显示,无清淋预处理的Neo-T疗法可能是治疗晚期实体瘤的一种安全、有前景治疗方案。

过继性T细胞疗法(adoptive T cell therapy,ACT)正在成为晚期肿瘤患者有前景的治疗选择。这些过继细胞包括嵌合抗原受体(CAR) T 细胞、T 细胞受体(TCR)T 细胞和肿瘤浸润淋巴细胞(TIL)。多项临床研究表明,新抗原特异性肿瘤浸润淋巴细胞(TIL)的过继转移可以介导几种实体肿瘤的持久消退。然而,收集TIL需对肿瘤组织进行侵入性取样,且通常受到切除肿瘤组织尺寸相对较小的限制,此外,某些肿瘤部位难以取样。最近,有研究报道称,在肿瘤患者外周血中发现了可识别新抗原的T细胞克隆。并且外周血淋巴细胞(peripheral blood lymphocyte,PBL)中的T细胞可识别新抗原P53,如同TILs。因此,本研究推测PBL可能成为获取T细胞的可靠且无创的来源,用于开发靶向新抗原ACT疗法来治疗肿瘤患者。
非清髓性清淋化疗常用于ACT之前以抑制宿主免疫系统,降低免疫原性,从而提高IL2,IL7,IL15等的可用性,减少调节性T细胞(Treg),并增加回输T细胞的持久性。氟达拉滨和环磷酰胺是清淋化疗最常用的药物。然而,清淋也会引起神经毒性、中性粒细胞减少、贫血和感染风险增加等不良反应。目前,清淋的给药强度在不同的中心和临床试验中差异较大,并且每个T细胞产品都有各自特有的清淋方案,尚缺乏标准清淋方案。
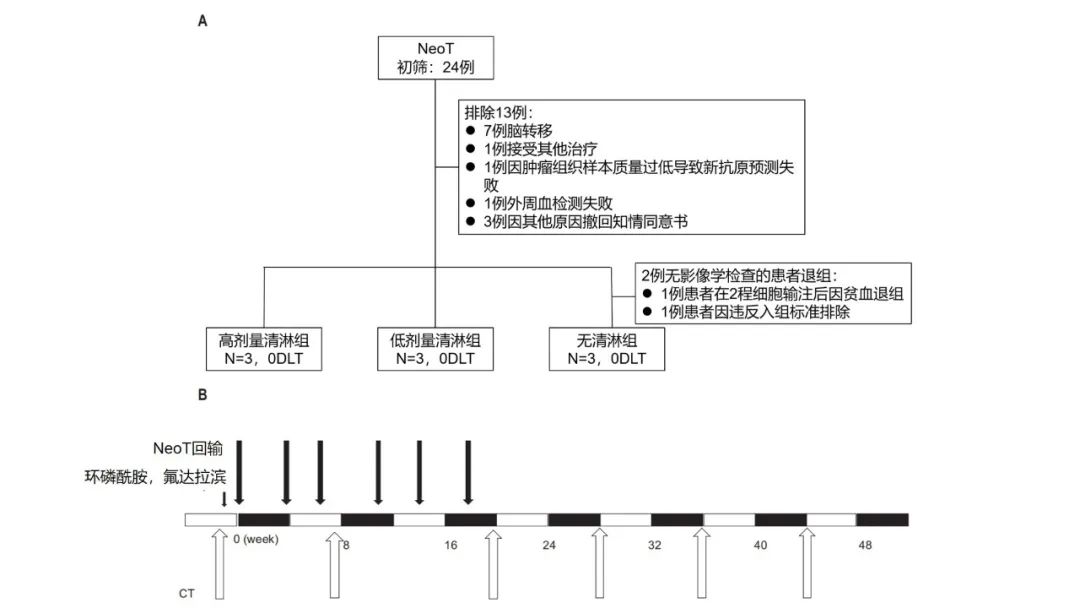
研究过程图示
在本研究中,研究者开发了一种从患者外周血单核细胞中产生个性化Neo-T(新抗原特异性CD8+T细胞)的方法。首先,建立了一个管道,包括通过生物信息学分析进行新抗原预测,并在25天内对T细胞大规模扩增特异性新抗原。为了评估Neo-T治疗的临床疗效并确定Neo-T治疗时的最佳清淋强度,研究者以氟达拉滨和环磷酰胺剂量递增的方式对Neo-T疗法进行了首次人体研究。本研究共纳入了11例标准治疗难治性局部晚期或转移性实体瘤患者,按照入组时间分为三个治疗组:无LD化疗预处理组、低强度LD化疗预处理组和高强度LD化疗预处理组。
研究结果显示,所有入组患者的PBMC均成功产生Neo-T,并可成功识别几种预测的新抗原。尽管Neo-T治疗输注剂量相对较小(4.78E7-9.0E8),但仍展现出有希望的客观缓解率(33%),与输注T细胞数量为1E10-1E11的TIL/TCR-T疗法疗效相当。出乎意料的是,无清淋化疗预处理组的患者临床反应最佳。
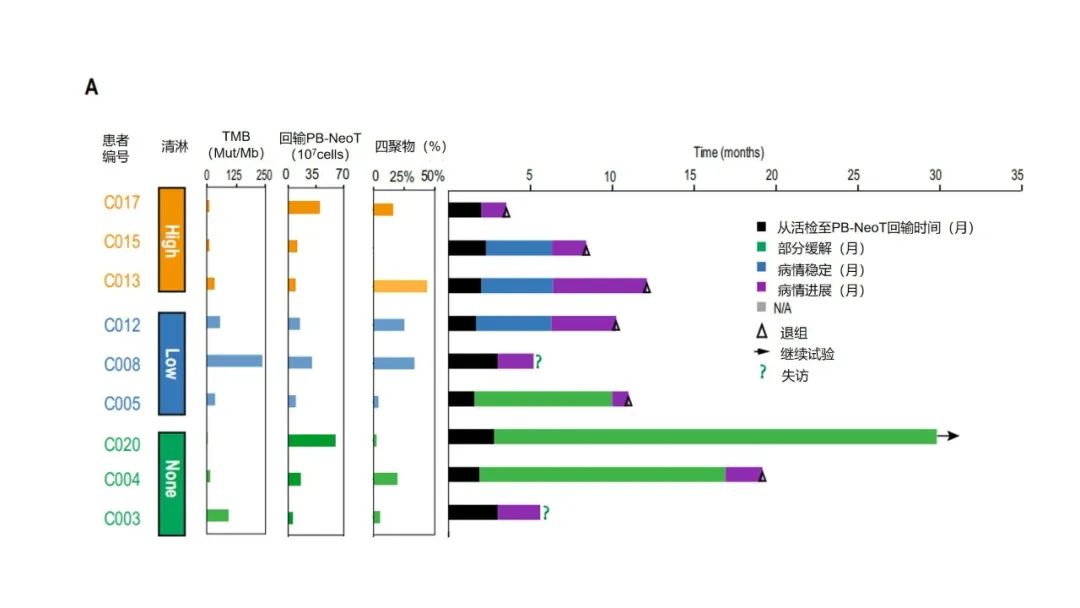
三个治疗组研究结果对比
在安全性方面,最常见的不良反应包括贫血、淋巴细胞减少、蛋白尿、瘙痒、皮疹、窦性心动过速等。3-4级不良反应多发生于低强度LD化疗预处理组和高强度LD化疗预处理组,最常见是淋巴细胞减少。未发生急性不良事件,总体而言,安全性良好。
综上,本研究表明,经由肿瘤患者外周血制备个性化Neo-T过继转移治疗过程中,不同的清淋化疗剂量耐受性良好,安全可控。并且在无清淋化疗预处理情况下仍能够介导持久的肿瘤消退。
中山大学肿瘤防治中心(华南恶性肿瘤防治全国重点实验室)徐瑞华教授、张晓实教授以及深圳华大基因研究院张曦研究员为该研究论文的共同通讯作者。中山大学肿瘤防治中心李丹丹副主任医师、李婧婧副主任医师、丁娅副主任医师及深圳华大基因研究院陈超、岳建辉、王海伦为共同第一作者。

通讯作者 徐瑞华
医学博士,中山大学肿瘤防治中心主任、医院院长、研究所所长,中国医学科学院学部委员,华南恶性肿瘤防治全国重点实验室主任,教授,博士生导师。中国临床肿瘤学会理事长,中国抗癌协会副理事长,中国抗癌协会靶向治疗专委会首届主任委员,中国抗癌协会化疗专委会候任主任委员,中国临床肿瘤学会肠癌专委会主任委员,《Cancer Communications》主编,研究生教材《肿瘤学》主编,本科生教材《临床肿瘤学》主编。徐瑞华作为通讯或第一作者在国际顶级期刊JAMA、Nature Materials、Cancer Cell、Lancet Oncology等发表SCI论文200余篇,入选科睿唯安(Clarivate Analytics)全球高被引科学家,连续入选中国高被引学者榜单;以第一完成人获国家科技进步二等奖2项、全国创新争先奖、省部级一等奖6项、吴阶平医学创新奖、谈家桢临床医学奖;入选全国先进工作者、国家百千万人才工程、国务院特殊津贴专家、南粤百杰人才培养工程、国家卫生计生突出贡献中青年专家等人才项目。

共同通讯作者 张晓实
医学博士,教授,主任医师。中山大学肿瘤防治中心生物治疗中心副主任,黑色素瘤单病种首席专家,广东省抗癌协会黑色素瘤专委会名誉主任委员,广东省临床医学学会肿瘤免疫治疗专委会主任委员,中国临床肿瘤学会(CSCO)黑色素瘤专委会副主任委员等。以通讯作者发表高水平论文多篇,包括Cell research、Nature communications、Eur J Cancer、Front Immunol等,主持国家自然科学基金3项,省级科研课题5项,主编出版《肿瘤生物治疗学》、《黑色素瘤基础与临床》和《黑色素瘤》等专著。

第一作者 李丹丹
医学博士,中山大学肿瘤防治中心生物治疗中心副主任医师。广东省临床医学学会肿瘤免疫治疗专委会常委、广东省抗癌协会黑色素瘤专委会委员、广东省抗癌协会遗传性肿瘤专委会委员、广东省健康管理学会肿瘤防治专委会常委等。以第一作者/共同通讯作者在Cell Research、Nat Commun、Autophagy、Oncogene、Front Immunol等发表多篇论文,主持并完成多项国家自然科学基金、广东省自然科学基金项目。

共同第一作者 李婧婧
医学博士,中山大学肿瘤防治中心生物治疗中心副主任医师。以第一作者/共同通讯作者在Nat Commun、Front Immunol、J Immunol、Front Oncol、J Allergy Clin Immunol等发表多篇论文,主持参与多项国家自然科学基金及省级科研课题。

共同第一作者 丁娅
医学博士,中山大学肿瘤防治中心生物治疗中心副主任医师。广东省抗癌协会黑色素瘤专委会常委、广东省健康管理协会肿瘤防治专委会常委、广东省医院协会肿瘤生物治疗专委会秘书等。以第一作者/共同通讯作者在Nat Commun、Front Immunol、J Allergy Clin Immunol等发表多篇论文,主持参与多项国家自然科学基金及省级科研课题。