


2026年3月12日,中山大学肿瘤防治中心孙颖、吕佳蔚团队在国际顶级期刊《自然》(Nature)发表了题为“Risk-adaptive Therapy Guided by Dynamic ctDNA in Nasopharyngeal Carcinoma”(基于动态ctDNA监测的鼻咽癌风险适应性治疗策略)的重磅研究成果(点击阅读原文查看)。该工作以鼻咽癌作为疾病模型,首次提出并验证了基于动态液体活检的“风险适应性治疗”新策略——在治疗过程中通过液体活检动态、无创地监测患者循环肿瘤DNA,实时更新患者的预后风险;同时结合患者肿瘤微环境的重塑特征“随机应变、因地制宜”地调整后续治疗方案,最终使患者获得真正的个体化精准治疗,从而延长生存时间。研究将鼻咽癌的治疗由过去“一成不变”的静态策略转变为“随机应变”的动态、个体化治疗决策。这也是该团队在鼻咽癌精准诊疗领域取得的又一里程碑式突破。

临床困境:治疗“一成不变”,风险却在动态改变
各种抗肿瘤治疗(如放疗、化疗、靶向治疗等)在缩小肿瘤的同时也会触发肿瘤细胞自身及其所在微环境不断演进。值得注意的是,这些改变反过来又会进一步影响抗肿瘤治疗疗效和患者的长期预后。这意味着,患者的复发转移风险并非一成不变,而是随着治疗的进行动态改变。
然而长期以来,肿瘤患者的治疗方案通常是治疗开始前就“固定好”的:所有患者按照指南的推荐接受固定的治疗。这显然与其动态变化的复发转移风险是矛盾的。这样的治疗模式导致一部分对治疗敏感的低风险的患者可能被“过度治疗”,承受了不必要的毒副作用;而另一部分对治疗不敏感的高风险患者则可能因标准治疗强度不足而错失最佳干预时机,最终导致治疗失败。这是目前临床医生日常工作中面临的痛点和困境。
尽管这一问题困扰临床医生已久,却一直没有很好的解决办法,其根源在于:能够指征患者动态预后风险的分子指标未知;无创、高效实现这一过程的技术路径未知;结合分子指标实时变化指导精准治疗的策略方案未知;患者能否从精准诊疗中真正获益的临床价值未知。这些环环相扣的问题是领域内长期悬而未决的重要问题。
破局思路:抓住“机会窗”,利用ctDNA进行无创、动态“考核”
为了填补这一空白,孙颖/吕佳蔚团队率先找到了能够指征患者动态预后风险的无创分子指标,揭示了治疗过程中血浆游离Epstein-Barr病毒DNA(cfEBV DNA)可以作为反映鼻咽癌患者治疗响应性和复发转移风险的可靠、实时、无创的生物学标记,研究于2024年发表在Cancer Cell杂志(“EP-SEASON”研究)。
然而,如何进一步将这些动态液体活检信息转化为指导临床决策的行动指南依旧困扰着临床医生?团队在此基础上进一步设计并开展了一项名为“EP-STAR”的多中心、II期适应性临床试验。研究者不再对所有患者“一视同仁”,而是利用诱导化疗带来的“机会窗”,通过cfEBV DNA的动态变化对患者的治疗响应性和复发转移风险进行实时的“监测”和“考核”,并根据考核结果“随机应变”“因地制宜”地调整后续治疗方案(图1)。
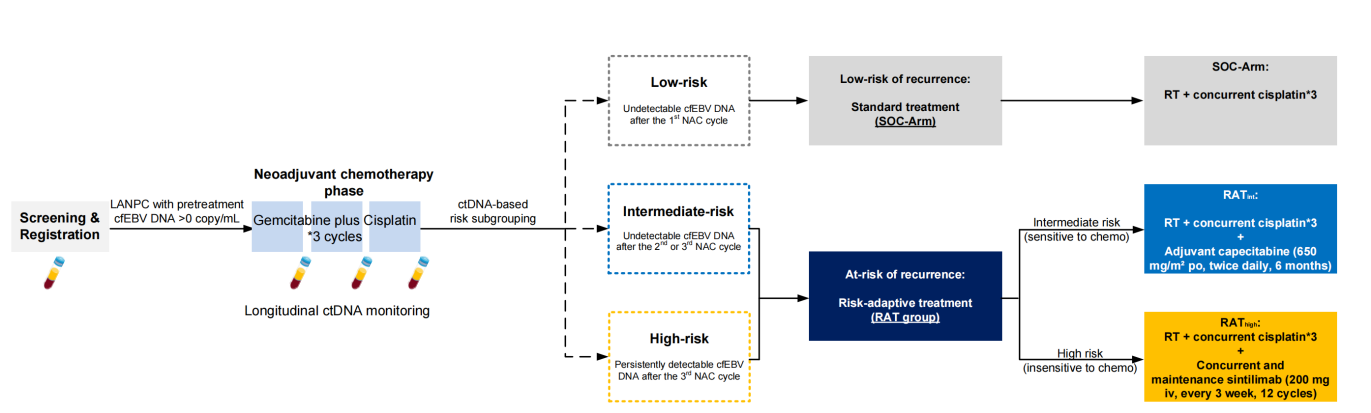
图1. 研究设计
如何“随机应变”?
首先,所有入组的局部晚期鼻咽癌患者均先统一接受3个疗程的标准GP方案诱导化疗;在这一“window-of-opportunity机会窗”中,团队根据cfEBV DNA的动态清除规律将患者精准划分为三个风险等级:
低风险组(Low risk):1个疗程化疗后患者的cfEBV DNA即迅速清零,预后极佳;因此继续接受标准治疗,不再进行风险适应性治疗调整以及治疗强度的增加。
中风险组(Intermediate risk):2-3个疗程化疗后患者的cfEBV DNA才清零,肿瘤负荷大预后相对差;因此后续进行风险适应性治疗调整(RATint)。
高风险组(High risk):3个疗程化疗后患者的cfEBV DNA仍未清零,复发转移风险极高;因此后续进行风险适应性治疗调整(RAThigh)。
如何“因地制宜”?
接下来,研究团队发现各ctDNA风险亚组在GP化疗后呈现出截然不同的肿瘤微环境重塑特征(图2):
低风险组(Low risk):GP化疗后表现为抗肿瘤免疫持续激活,支持了其预后极佳的临床结局。
中风险组(Intermediate risk):GP化疗后微环境中富集了大量干性肿瘤细胞;因此调整治疗方案为在标准放化疗后加用能够有效杀伤干细胞的节拍卡培他滨进行强化治疗。
高风险组(High risk):GP化疗后微环境中的T细胞呈现大量耗竭状态;因此调整治疗方案为在放疗伊始即联合信迪利单抗(anti-PD-1免疫治疗)并持续至辅助治疗阶段共维持12个周期。
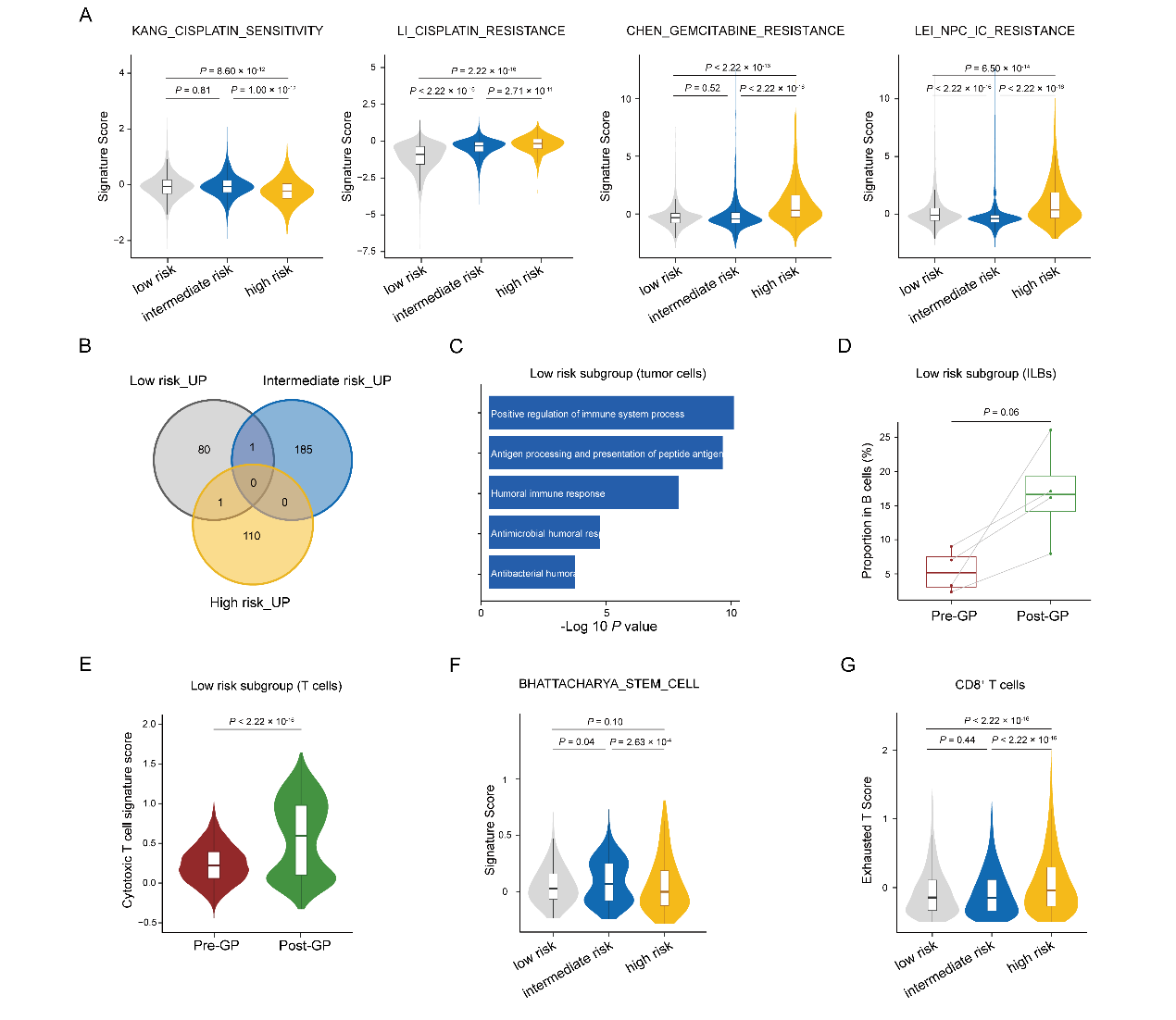
图2. GP化疗重塑各ctDNA风险组患者的肿瘤微环境
临床结局:显著降低疾病进展风险,兼具卫生经济学效益
经过中位47.3个月的随访,接受“随机应变、因地制宜”治疗策略的中高危患者(RAT group),3年无失败生存率达89.1% (95%CI: 83.2–95.0%):其中“中风险”组患者的3年无失败生存为91.4% (95%CI: 84.1–98.7%);而传统上认为预后最差的“高风险”组患者的3年无失败生存率也达到了86.5% (95%CI: 77.3–95.7%)。平行地,“低风险”组接受标准治疗患者的3年无失败生存率为90.6% (95%CI: 80.4–100.0%)。
值得注意的是,与来自前瞻性EP-SEASON队列中相同风险但未接受适应性治疗的患者相比,这一策略将患者的疾病进展或死亡风险显著降低了59%(风险比HR = 0.41, 95%CI = 0.23–0.75, P = 0.004)(图3)。
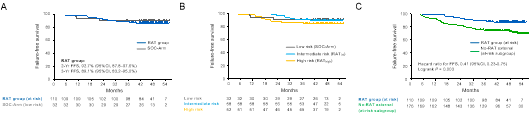
图3:疗效分析
安全性数据方面,该策略展现出良好的临床安全性,且不牺牲患者的生活质量。更重要的是,马尔可夫模型显示,该策略虽然在总成本上增加了2404.1美元,但其提升了1.9个质量调整生命年(QALY),增量成本-效果比(ICER)为每QALY 1225.2美元,远低于公认的37672美元/QALY的支付意愿阈值,兼具卫生经济学效益(表1)。
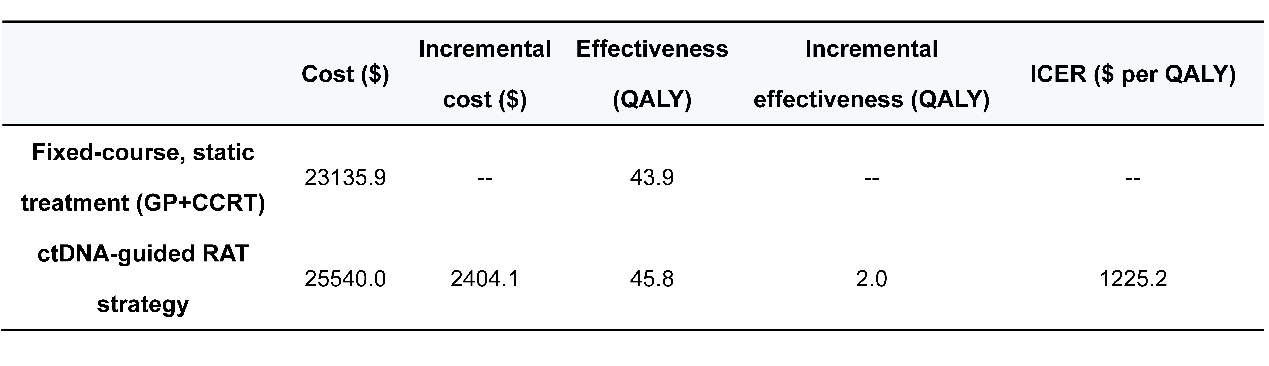
表1. 基于马尔可夫模型的卫生经济学分析
该研究入选美国临床肿瘤学年会口头报告,是国际上首个发表的动态ctDNA指导下的适应性临床试验。Nature杂志同期以临床简报(Clinical Briefing)的形式重点报道(Highlight)该研究(Clinical Briefing为Nature杂志旗下板块,将最具前沿的、具有重大临床转化潜力的科学研究以一种能够迅速理解、吸收并可能应用于实践的方式进行报道和呈现)。杂志副主编Victoria Aranda在述评中指出:研究为ctDNA及个体化治疗领域提供了极具价值的全新见解,不仅限于EB病毒相关的鼻咽癌,更对后续临床试验设计及临床实践转化均具有里程碑式的指导意义与深远影响。

该研究在国家自然科学基金委创新研究群体项目(A类)的资助下完成。中山大学肿瘤防治中心孙颖教授、马骏院士、周冠群主任医师、李济宾研究员为该论文的共同通讯作者。中山大学肿瘤防治中心吕佳蔚副主任医师、郑丹雪博士、梧州红十字会医院梁锦辉教授、佛山市第一人民医院张宁教授、中山大学肿瘤防治中心叶祖禄副主任技师、许旭东博士、新加坡国立癌症中心Melvin L.K. Chua教授为共同第一作者。
研究者简介:

通讯作者:孙颖 教授
中山大学肿瘤防治中心副主任、副院长,二级教授,国家重大人才工程入选者、享受政府特殊津贴专家、人社部国家百千万人才工程“有突出贡献中青年专家”、科技部创新人才推进计划-中青年科技创新领军人才。现任中国抗癌协会第九届理事会理事,中国临床肿瘤学会(CSCO)鼻咽癌专委会副主任委员,中国抗癌协会肿瘤大数据与真实世界研究专委会副主任委员等职。作为联合主席牵头制定了《中国-美国临床肿瘤学会鼻咽癌临床诊治国际指南》;近5年来,作为通讯/一作(含共同)发表高水平论著50余篇,包括Nature、N Engl J Med、Lancet、JAMA、BMJ、Nat Med、Cancer Cell、Lancet Oncol、JCO、Radiology、Nat Commun等;主持国家重点研发计划项目1项、国自然重大研究计划重点支持项目1项、国自然数学天元基金数学与医疗健康交叉重点专项1项及国自然基金面上项目4项;发明专利已授权15项,转让5项;作为主要完成人之一获国家科技进步二等奖3项,省部级科技奖一等奖8项。

第一作者:吕佳蔚 副主任医师
获得国家自然科学基金青年基金项目B类、博士后创新人才支持计划资助。发表一作/通讯(含共同)高水平论文多篇,包括Nature、Nat Med、Cancer Cell、Nat Commu、Sci Adv、Ann Oncol、BMC Med、Oncogene等;其中1篇论文入选ESI TOP 1%高被引论文。