朱孝峰教授团队发现调控神经母细胞瘤分化的重要机制和新靶标
2017/10/31 15:02:03 来源: 阅读数:5265
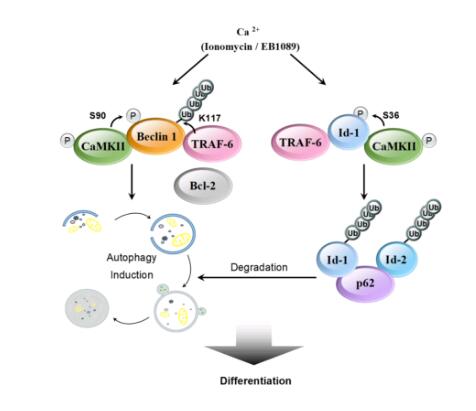
10月27日,朱孝峰教授团队在《Nature Communications》杂志上发表题为“CaMKII-mediated Beclin 1 phosphorylation regulates autophagy that promotes degradation of Id and neuroblastoma cell differentiation”(文章链接:https://www.nature.com/articles/s41467-017-01272-2)的研究论文,揭示了钙调蛋白激酶CaMKII介导Beclin 1磷酸化进一步促进其发生K63型泛素化并激活自噬,从而加速分化抑制蛋白Id1和Id2的降解,导致神经母细胞瘤分化。
神经母细胞瘤是儿童最常见的颅外肿瘤,约占儿童肿瘤的6-10%,占儿童肿瘤死亡的15%。神经母细胞瘤具有高度未分化的特性,对于高危型患儿的治疗进展缓慢,需要寻找更加有效的治疗策略。自噬是细胞在物质能量缺乏或外环境压力下,生物大分子或细胞器经双层膜结构囊泡包裹并被大量降解的过程。自噬与恶性肿瘤发生发展的关系是近年来学界所关注的热点问题。自噬在细胞分化中的作用鲜为报道,朱孝峰教授研究团队发现钙调蛋白激酶CaMKII可以直接磷酸化Beclin 1的丝氨酸90位点,并促进后者发生K63型泛素化进而激活自噬,同时,CaMKII也可以磷酸化分化抑制蛋白Id1和Id2,磷酸化的Id蛋白进而与泛素连接酶TRAF6结合,促进Id蛋白的K63型泛素化,泛素化的Id1和Id2通过与自噬受体P62的结合被带入到自噬体中降解。Id蛋白的降解促进了神经母细胞瘤细胞分化,从而达到抑制肿瘤的目的。
这一研究揭示了CaMKII激活到Id蛋白的自噬性降解进而调控细胞分化的分子机制,为临床上神经母细胞瘤靶向治疗提供了新的靶标。
该研究工作的第一作者为中山大学肿瘤防治中心李轩博士、吴晓琦博士、邓蓉副研究员,通讯作者是朱孝峰教授。该项目获得了国家自然科学基金、973计划以及华南肿瘤学国家重点实验室等基金和单位的支持。